پراکسید هیدروژن به دلیل ساختار مولکولی خود یک ماده بسیار منحصر به فرد است. برخلاف بسیاری از مواد که اکسیژن در حالت اکسیداسیون ۰ یا ۲- وجود دارد، از اتمهای اکسیژن در حالت اکسیداسیون ۱- تشکیل شده است. این بدان معناست که این ماده بسته به PH محلول آن می تواند هم به عنوان اکسید کننده و هم به عنوان عامل کاهنده استفاده شود. در این مقاله بیشتر در مورد فرمول تجزیه آب اکسیژنه خواهیم گفت.پراکسید هیدروژن یک ماده کاملاً پایدار در pH کم و متوسط است. اگرچه آنیون های هیدروکسیل نمی توانند به تنهایی واکنش را تحریک کنند، افزایش قلیالیت در محیط واکنش تا یک مقدار معین ممکن است منجر به افزایش سرعت واکنش شود. متأسفانه تأثیر pH بر سرعت واکنش به شدت به خلوص محلول بستگی دارد. به عنوان مثال، در یک محلول با خلوص پایین، pH ممکن است به هیچ وجه بر آن تأثیر نگذارد. با این حال، H2O2 هنگامی که در معرض ناخالصی ها یا کاتالیزورهایی مانند سطوح فلزی یا مخمر قرار می گیرد، به راحتی تجزیه می شود.
آب اکسیژنه چیست ؟
این یک تک پیشران است که وقتی خالص می شود، در دماهای بالا یا زمانی که یک کاتالیزور وجود دارد، خود تجزیه می شود. پراکسید هیدروژن که تنها برای تولید اکسیژن و آب تجزیه می شود. یکی از تمیزترین و همه کاره ترین مواد شیمیایی موجود است. تجزیه کاتالیستی پراکسید هیدروژن امکان استفاده از کاتالیزورهای مختلف را فراهم می کند که سرعت تجزیه را افزایش می دهد.
پراکسید هیدروژن، در صنعت نساجی، به عنوان سفید کننده و خوشبوکننده منسوجات، خمیر چوب، مو، خز و … استفاده می شود. کاربردهای دیگر H2O2 به عنوان منبع پراکسیدهای آلی و معدنی، سوخت موشک، نرم کننده، عامل خنثی کننده در تقطیر شراب، سفید کننده و عامل اکسید کننده در غذاها است.
💡 مقاله پیشنهادی ما : آب اکسیژنه خوراکی است؟
حال که دانستیم آب اکسیژنه چیست بهتر است فرمول تجزیه آب اکسیژنه هم بدانید.
فرمول تجزیه آب اکسیژنه چیست؟
هیدروژن پراکسید، به کندی در غیاب کاتالیزور تجزیه می شود. ولی در محیط بازی و در حضور کاتالیزورهایی همچون نقره، منیزیم دی اکسید و پلاتین به سرعت تجزیه می شوند. اکسیژن و آب محصولات این تجزیه هستند. سرعت تجزیه هیدوژن پراکسید به عواملی همچون دما، pH و غلظت بستگی دارد.
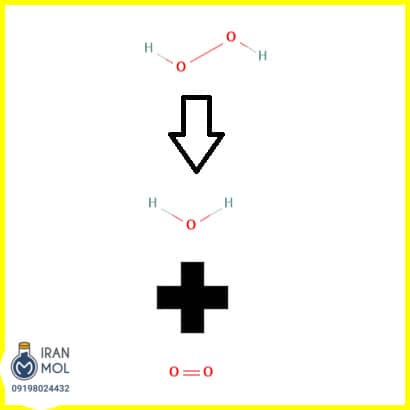
معادله تجزیه آب اکسیژنه (هیدروژن پراکسید) در زیر آورده شده است.
![]()
معادله تجزیه آب اکسیژنه
عوامل دیگری که بر سرعت واکنش تأثیر می گذارند. عبارتند از :
دما، فشار، غلظت محلول، نوع، فعالیت و سطح سطح کاتالیستی فعال کاتالیزور، قرار گرفتن در معرض نور مستقیم خورشید و وجود بازدارنده ها
واکنش تجزیه پراکسید هیدروژن در دماهای متوسط و بدون حضور کاتالیزور بسیار کند است. با افزایش دما می توان سرعت آن را افزایش داد، که باعث واکنش تجزیه حرارتی می شود.
این واکنش را می توان در فاز مایع یا بخار انجام داد. معمولا سرعت واکنش با افزودن کاتالیزور به راکتور افزایش می یابد. تقریباً همه انواع کاتالیزور را می توان با این واکنش استفاده کرد :
- ناهمگن (به عنوان مثال نقره، طلا، آهن)
- همگن (یون های یدید یا آهن)
- آنزیم ها (کاتالاز)
استفاده از فرمول تجزیه آب اکسیژنه
در بسیاری از صنایع از تجزیه پراکسید هیدروژن برای تولید سدیم پربورات و پرکربنات سدیم (مواد سفید کننده در مواد شوینده جامد و مایع) استفاده می شود.
خطرات
قرار گیری طولانی مدت پراکسید هیدروژن (با نام علمی آب اکسیژنه) در مجاورت آتش و حرارت، موجب تجزیه آن می شود. علاوه بر این، این مواد در تماس با مواد قابل احتراق، به طور خود به خودی منفجر می شوند. بنابراین، همواره دور از نور و در محیط های خشک و خنک ذخیره و نگهداری می شود.
💡 برای مطالعه مضرات آب اکسیژنه کلیک کنید.
سخن آخر
پراکسید هیدروژن یک ماده شیمیایی است که در مصارف زیر استفاده می شود.
- در واکنش های اکسیداسیون، تصفیه آلاینده های مختلف معدنی و آلی، فرآیندهای سفیدکننده در صنایع خمیر کاغذ، کاغذ و نساجی و برای کاربردهای مختلف ضد عفونی
فرمول تجزیه آب اکسیژنه (electrolysis of water) را مشاهده کنید.
۲H2O (آب) → ۲H2 (هیدروژن گاز) + O2 (اکسیژن گاز)
در این مقاله برای شما گفتیم که آب اکسیژنه چیست. اگر به اطلاعات بیشتر در مورد آب اکسیژنه نیاز دارید کلیک کنید. جهت اطلاع از قیمت آب اکسیژنه با ما، ایران مول در تماس باشید.
پرسش و پاسخ متداول
مشتاقانه آماده پاسخ گویی به سوالات علمی و تخصصی شما هستیم.
معادله شیمیایی تجزیه آب اکسیژنه (H2O2) به آب (H2O) و اکسیژن (O2) چیست؟
معادله این واکنش تجزیه به صورت زیر نوشته می شود. ۲ H2O2 → ۲ H2O + O
h2o2 → H2O O2 چه نوع واکنشی است؟
واکنش تجزیه واکنش تجزیه زمانی رخ می دهد که یک واکنش دهنده به دو یا چند محصول تجزیه شود. معادله کلی آن به صورت زیر نشان داده شده است: AB → A + B نمونه هایی از واکنش های تجزیه شامل تجزیه پراکسید هیدروژن به آب و اکسیژن، و تجزیه آب به هیدروژن و اکسیژن است.
۲ محصول حاصل از تجزیه پراکسید هیدروژن کدامند؟
واکنش پراکسید هیدروژن، از نظر ترمودینامیکی ناپایدار است. در دماها و غلظت های بالاتر تجزیه شده و آب و اکسیژن را تشکیل می دهد.